Monde
Covid-19: les États-Unis autorisent le traitement Evusheld d'AstraZeneca
10/12/2021 - 07:00
SNRTnews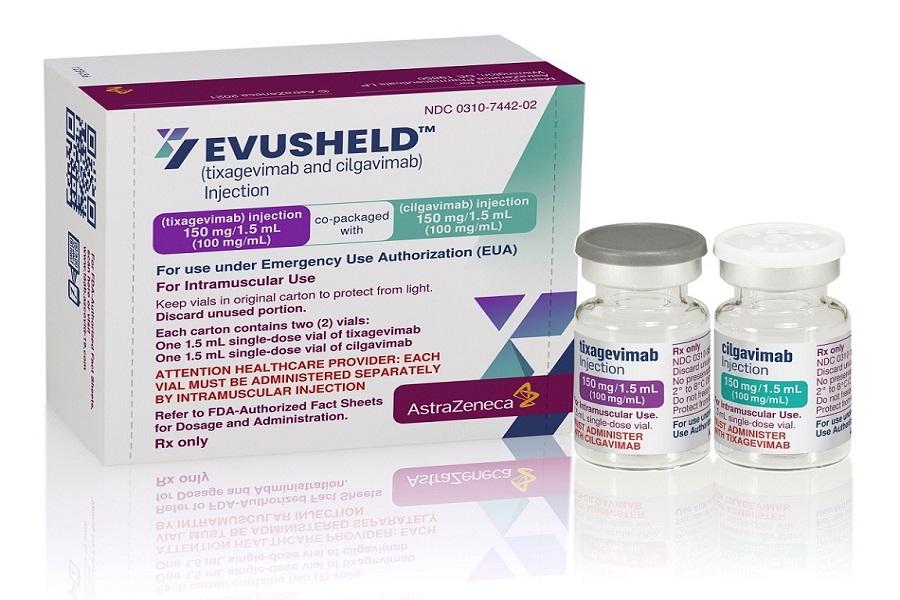
Le traitement Evusheld d'AstraZeneca (tixagevimab associé au cilgavimab), qui est une combinaison d'anticorps à action prolongée (LAAB), vient d’être autorisé en urgence (EUA) aux États-Unis pour la prévention contre COVID-19. Les premières doses de ce traitement seront disponibles prochainement.
Il s’agit du seul traitement par anticorps à avoir été autorisé aux États-Unis pour la prévention, lit-on dans un communiqué parvenu à l’équipe de SNRTNews. The Food and Drug Administration (FDA) a ainsi autorisé Evusheld pour la prévention de l'exposition au COVID-19 chez les adultes et les adolescents (âgés de 12 ans et plus et pesant 40 kg ou plus) avec une immunité modérée à sévère. Ce sont surtout les personnes qui pourraient ne pas présenter une réponse immunitaire adéquate à la vaccination contre la Covid-19 ainsi que ceux pour qui elle n’est pas recommandée.
Une alternative pour ceux qui ne peuvent pas se faire vacciner
"Des millions de personnes aux Etats-Unis et dans le monde entier demeurent toujours autant exposées à un risque sérieux de contracter le COVID-19, en raison de leur système immunitaire qui ne génère pas de réponse immunitaire suffisante, et ce même après avoir reçu toutes les doses recommandées de vaccin", explique Myron J. Levin, MD, professeure de pédiatrie et de médecine à l'école de médecine de l'Université du Colorado (États-Unis). Elle fait également part de son enthousiasme quant à l'autorisation d’Evusheld aux Etats Unis. "Ce traitement par anticorps est très facile à administrer et offre une protection durable qui est à même de permettre à ces personnes de retrouver une vie normale."
Pour sa part, Mene Pangalos, Vice-président exécutif, R&D BioPharmaceutique, AstraZeneca, a déclaré que grâce à Evusheld, ils allaient pouvoir avoir désormais accès à la première thérapie par anticorps autorisée aux États-Unis et qui permettra de lutter beaucoup plus efficacement contre le COVID-19. "A ce jour, Evusheld neutralise toutes les variantes du SARs-CoV-2, et nous œuvrons rapidement pour établir son efficacité contre la nouvelle variante Omicron. Nous remercions les participants à nos essais cliniques, mais aussi les investigateurs, les scientifiques et les agences gouvernementales, ainsi que nos collègues d'AstraZeneca, qui ont tous contribué au développement d'Evusheld", dit-il.
De son côté, Brian Koffman, MDCM (retraité), MS Ed, cofondateur, vice-président exécutif et directeur médical de la CLL (Chronic Lymphocytic Leukemia) Society, États-Unis, a fait savoir que ce traitement permettra à tous ceux qui ne peuvent pas compter sur la vaccination seule d’avoir toute la protection dont ils ont besoin. "En tant que médecin et personne dont le système immunitaire est affaibli, je suis rempli d'espoir maintenant qu'Evusheld est là."
Toujours selon le communiqué, Evusheld est une combinaison de deux anticorps monoclonaux à action prolongée. Il s’agit du seul traitement par anticorps autorisé aux États-Unis pour la prévention contre le COVID-19 qui est aussi le seul anticorps contre le virus administré par voie intramusculaire (150 mg de tixagevimab et 150 mg de cilgavimab).
Environ 2 % de la population mondiale présente un risque accru de réponse inadéquate aux vaccins COVID-19. Ceci concerne notamment des personnes atteintes de cancers du sang ou d'autres cancers traités par chimiothérapie, des patients sous dialyse et de ceux qui prennent des médicaments après une transplantation d'organe ou qui prennent des médicaments immunosuppresseurs pour des affections telles que la sclérose en plaques et la polyarthrite rhumatoïde.
Dans ce sens, Evusheld a été très bien toléré suite à tous les essais qui ont été réalisés. Les données primaires obtenues à l’issue de la phase III des tests effectués par PROVENT démontrent une réduction statistiquement significative (77% à l'analyse primaire, 83% à l'analyse médiane à six mois) du risque de développer une affection à la COVID-19 symptomatique (par rapport au placebo). A ceci, s’ajoute une protection contre le virus se poursuivant pendant au moins six mois après l’administration d’Evusheld. Mais un suivi accru est nécessaire pour établir la durée totale de la protection fournie par Evusheld.
Des premières doses offertes gratuitement
Des études sont en cours pour fournir des informations sur l'impact de la nouvelle variante Omicron (B.1.1.529) sur Evusheld. En effet, aucune des substitutions du site de liaison Omicron pertinentes pour Evusheld qui ont été testées à ce jour dans des essais précliniques n'a été associée à un échappement à la neutralisation d'Evusheld. Bien au contraire, les résultats obtenus en laboratoire démontrent qu'Evusheld neutralise d'autres variantes virales émergentes récentes du SRAS-CoV-2, y compris les variantes Delta et Mu.
S’exprimant à ce sujet, Rami Scandar, président, Proche-Orient et Maghreb, AstraZeneca, a déclaré que l'approbation par The Food and Drug Administration américaine d’Evusheld (anciennement AZD7442) pour la prévention du COVID-19 est une étape importante. "Nous nous réjouissons de cette nouvelle et de l'opportunité qu'elle nous offre de pouvoir répondre aux besoins non satisfaits des patients les plus vulnérables. Les données récentes de l'essai de phase III PROVENT ont démontré toute l'efficacité d’Evusheld ainsi que la capacité de protection qu’il est capable d’offrir auprès de patients à haut risque et immunodéprimés", souligne-t-il.
AstraZeneca a accepté de fournir au gouvernement américain 700 000 doses d'Evusheld. Ces premières doses d'Evusheld seront disponibles gratuitement pour les patients éligibles dans le cadre d'un programme spécifique financé par le gouvernement. L’entreprise avance dans le dépôt de dossiers à travers le monde entier, et ce en vue d'obtenir des autorisations d'utilisation d'urgence ou des approbations conditionnelles d'Evusheld.

Articles en relations
Monde
Monde
Société
Société